 我要收藏
公共资源调用站点
文章分享
我要收藏
公共资源调用站点
文章分享

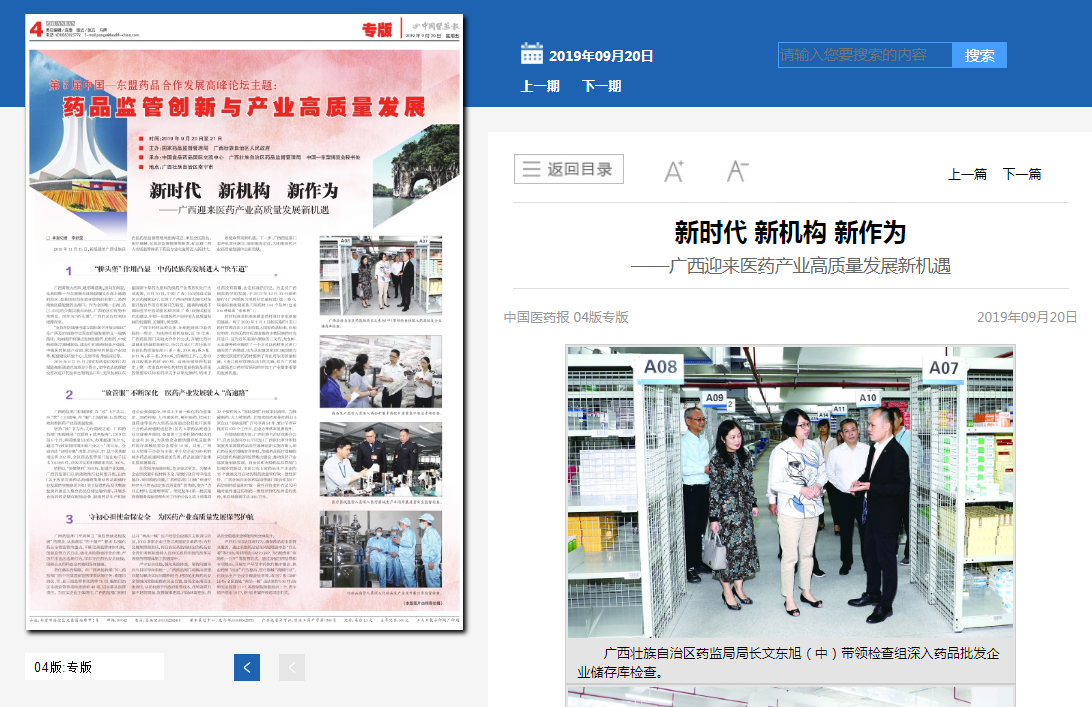
广西壮族自治区药监局局长文东旭(中)带领检查组深入药品批发企业储存库检查。

药品生产监管人员深入药企开展中药饮片质量集中整治专项检查。

医疗器械监管人员深入医疗器械生产车间开展质量安全监督检查。

化妆品监管人员深入化妆品生产企业开展日常监督检查。
本报记者 李舒雯
2018年11月15日,新组建的广西壮族自治区药品监督管理局挂牌成立,承担全区药品、医疗器械、化妆品监督管理等职责,标志着广西大市场监管体系下药品专业化监管迈入新时代。
新使命带来新机遇。下一步,广西药监部门将严抓责任落实、靠前服务企业,为助推医药产业高质量发展作出新贡献。
“桥头堡”作用凸显 中药民族药发展进入“快车道”
广西背靠大西南,毗邻粤港澳,面向东南亚,是我国唯一与东盟既有陆地接壤又有海上通道的地区,是我国面向东盟开放的前沿窗口,是西南地区最便捷的出海口。作为全国唯一沿海、沿江、沿边的少数民族自治区,广西的区位优势非常明显。而作为“桥头堡”,广西的区位红利也接踵而至。
“支持在防城港市建立国际医学开放试验区”是广西及防城港市实现高质量发展的又一战略路径。防城港市将重点发展创新药、仿制药、中成药和医疗器械制造,建设中印医药制造产业园、中俄医药制造产业园、欧美新特药制造产业园等,配套建设研发中心、交易市场、物流园区等。
2019年8月15日,国家发改委印发的《西部陆海新通道总体规划》提出,支持依法依规建设首次进口药品和生物制品口岸、支持发展以东盟国家中草药为原料的医药产业等系列先行先试政策。8月30日,中国(广西)自由贸易试验区正式揭牌运行,实现了广西由西南边陲向对东盟开放合作前沿和窗口的转变。随着防城港市国际医学开放试验区和中国(广西)自贸试验区启动建设,中国—东盟医药产业将进入高质量发展的机遇期、关键期、黄金期。
广西中药材品种众多,壮瑶药是其中最亮眼的一部分。为扶持壮瑶药发展,近10年来,广西药监部门采取大合作的方式,开展壮药材基础和质量控制研究,先后完成《广西壮族自治区壮药质量标准》(第一卷,2008版;第二卷,2011版;第三卷,2018版)的编制工作,三卷标准共收载壮药材490种。这是壮瑶医药发展史上第一次由政府将壮药材的质量检验及质量控制要求以标准的形式予以制定颁布,结束了壮药没有典籍、法定标准的历史。为支持广西瑶医药学的发展,于2013年12月31日颁布施行《广西瑶族习用药材质量标准(第一卷)》,该卷标准收载瑶族习用药材144个品种(包括104种瑶医“老班药”)。
药材标准及标准来源是药材进口审批备案的基础。将于2020年1月1日起实施的《进口药材管理办法》对未收载入国家药品标准,但相应的省、自治区药材标准收载的少数民族药材允许进口。这为近年来国内紧缺的三叉苦、龙血树、大血藤等药材提供了一个正式以药材形式进口通关的广西渠道,也为从东盟国家进口我国南方少数民族使用的药材提供了有法可依的质量标准。《进口药材管理办法》的实施,将为广西做大做强进口药材贸易和药材加工产业提供重要的发展机遇。
“放管服”不断深化 医药产业发展驶入“高速路”
广西药监部门积极探索,在“放”上下功夫、在“管”上出重拳、在“服”上闯新路,以监管实效助推医药产业高质量发展。
坚持“放”字为先,力行简政之道。广西药监部门积极推进“互联网+政务服务”,2019年前6个月,承诺提速53.06%,办理提速76.31%,超过“行政审批时限压缩三分之一”的目标。全面启动“证照分离”改革,自治区、市、县三级共取消证明202项,全区药品监管部门发出电子证书130366件,总体评议率和满意率均达100%。
坚持以“快捷便利”为目标,促进产业发展。广西药监部门以新政助推行业转型升级,出台《关于改革完善药品流通政策推动药品流通行业发展的实施意见》和《关于促进药品现代物流发展的意见》,整合药品仓储运输资源,开展多仓协同药品储存配送业务,鼓励药品生产和流通企业强强联合,形成上下游一体化的企业集团。国药控股、九州通医药、柳州医药、桂林汇通药业等区内大型药品流通企业获批开展第三方药品流通配送业务;区内5家药品流通企业完成兼并重组,备案第三方委托储存配送的企业有36家,为其他企业提供储存配送服务的医疗器械经营企业增至16家。目前,广西以大型骨干企业为主体、中小型企业为补充的城乡药品流通网络更加完善,药品流通行业集中度显著提高。
优化程序高效审批,急企业之所急。为解决企业因次要申报材料不全,导致行政许可申报反复办、来回跑的问题,广西药监部门打破“申请材料齐全且符合法定形式再受理”的传统,变为“边补正材料,边受理审核”。制定发布《第一批实施政务服务容缺受理有关工作的公告》,将3类事项17个要件列入“容缺受理”行政审批清单。为维威制药、大力神制药、北部湾制药和花红药业4家企业“容缺受理”许可申请54件,累计节省审批时间672个工作日,企业办事效率显著提升。
在鼓励政策方面,广西壮族自治区党委办公厅、自治区政府办公厅印发《广西深化审评审批制度改革鼓励药品医疗器械创新实施方案》,深化药品医疗器械审评审批,加强药品医疗器械临床试验机构建设和监管能力建设,推动医药产业高质量创新发展。自治区和市级药品监管部门加强协同联动,全区已有5家药品生产企业的16个批准文号启动仿制药质量和疗效一致性评价。广西壮族自治区药监局等部门联合印发《广西仿制药质量和疗效一致性评价奖补方法》,明确对最终通过仿制药一致性评价的品种进行奖补,单品种最高可达400万元。
守初心担使命保安全 为医药产业高质量发展保驾护航
广西药监部门牢固树立“强监管就是促发展”的理念,认真落实“四个最严”要求,以强化药品全程监管为重点,不断完善监管体制机制,创新监管方式方法,强化风险隐患排查治理,严厉打击违法违规行为,牢牢守住药品安全底线,保障公众用药安全有效和身体健康。
责任落实有保障。在广西各地各部门中,药监部门首个完成国家监管事项认领任务,梳理自治区、市、县三级监管事项清单75项,编制自治区本级监管事项检查清单48项,切实落实监管责任。为压实企业主体责任,广西药监部门组织召开“两品一械”生产经营企业落实主体责任会议,1000多家企业已签订质量安全承诺书;为夯实属地管理责任,将自治区药监局制定的药品安全责任考核制度纳入自治区政府印发的改革完善疫苗管理体制工作通知中。
严守安全底线,强化风险排查。坚持问题导向与目标导向相统一,广西药监部门将解决思想问题与解决实际问题相结合,把防范化解药品安全领域风险隐患摆在突出位置,督促企业落实主体责任,从而有效节约政府监管成本,扭转监管力量不足的局面,监管效率更高,市场环境更优,药品安全隐患排查效能得到全面提升。
严厉打击违法违规行为,确保药品安全监管全覆盖。通过采取药品安全风险隐患排查“回头看”等行动,用好用活GMP、GSP、飞行检查和“双随机、一公开”等监管方式。通过加强日常监管和专项整治,开展生产环节中药饮片集中整治、执业药师“挂证”行为整治、医疗器械“清网行动”、化妆品生产企业全覆盖检查等,收回7张GMP证书;全区查处“两品一械”违法案件516件;取缔无证经营11户,捣毁制假售假窝点1个,责令停产停业19户,将42件案件移送司法机关。
(本版图片由程奇拍摄)
文件下载:
关联文件: